Elementlerin isimleri ve sembolleri! Element sembolleri, element tablosu, elementlerin özellikleri, periyodik cetvel ve ilk 20 element!

Element, aynı cins atomlardan oluşan ve kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere verilen isimdir. Tüm elementlerin isimleri ve sembolleri öğrenciler tarafından merak edilmektedir. Toplamda 118 tane element bulunmaktadır. Şimdi sizlere bu elementlerin isimlerini ve sembollerini paylaşacağız. Ayrıca periyodik cetvel ve elementlerin özelliklerine de ulaşabilirsiniz...
Element nedir? Elementlerin özellikleri nelerdir? Elementlerin isimleri nelerdir? Periyodik cetvelde toplamda kaç element var? Periyodik tabloda yer alan tüm elementlerin sembolleri nelerdir? 1A, 2A, 3A, 4A, 5A, 6A, 7A ve 8A grubu elementleri nelerdir? B grubu elementleri nelerdir? Elementlerin sembolleri nedir? Karbon'un sembolü, Oksijen'in sembolü, Hidrojen'in sembolü nedir? Periyodik cetvelde kaç grup var? Detaylar elementler konu anlatımı ve ders notlarında...
ELEMENT NEDİR?
Element, aynı cins atomlardan oluşan ve kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere verilen isimdir.
Her farklı kimyasal element farklı atom numarasına sahiptir. Atom numarası atomdaki proton sayısını (çekirdek yükünü) gösteren sayıdır. Bir elementin böylece tüm atomlarında aynı sayıda proton bulunur. Proton sayıları aynı, nötron sayısı (kütle numaraları [= proton sayısı + nötron sayısı]) farklı atomlara izotop denir.
TOPLAM KAÇ TANE ELEMENT VARDIR?
Toplam 118 adet element bulunmuştur. Bunların 94 tanesi Dünya üzerinde doğal olarak bulunmaktadır. 80 adet element kararlı izotopa sahiptir. Bu elementler, atom numarası 43 ve 61 (teknetyum ve prometyum) dışında atom numarası 1'den 82'ye kadar olan atomlardır. Atom numarası 83 ve daha fazlası olan atomlar (bizmut ve fazlası) kesinlikle kararli değildirler ve radyoaktif özellikler barındırırlar. Atom numarası 83'ten 94'e kadar olanlar kararlı değillerdir.
İNSAN VÜCUDUNDA BULUNAN ELEMENTLER NELERDİR?
Bir element insan vücudunda yüzde miligram mertebesinde bulunursa bu elemente makroelement (majörelement, plastik element) denir. Diğerlerine nazaran daha az oranda (yüzde mikrogram mertebesinde) bulunanlara ise izelement (oligoelement, minörelement, katalitik element) adı verilir. Minörelementler genellikle enzim, hormon gibi vücutta önemli fonksiyonu olan maddelere bağlı olarak görev yaparlar.
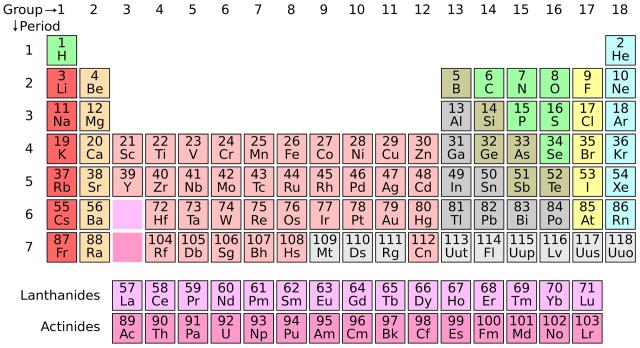
TÜM ELEMENTLERİN İSİMLERİ VE SEMBOLLERİ NELERDİR?
Toplamda 118 tane element mevcuttur. Şimdi bunların isimlerini ve sembollerini sırasıyla sizlere aktaralım.
1 : H : Hidrojen
2 : He : Helyum
3 : Li : Lityum
4 : Be : Berilyum
5 : B : Bor
6 : C : Karbon
7 : N : Azot
8 : O : Oksijen
9 : F : Flor
10 : Ne : Neon
11 : Na : Sodyum
12 : Mg : Magnezyum
13 : Al : Alüminyum
14 : Si : Silisyum
15 : P : Fosfor
16 : S : Kükürt
17 : Cl : Klor
18 : Ar : Argon
19 : K : Potasyum
20 : Ca : Kalsiyum
21 : Sc : Skandiyum
22 : Ti : Titanyum
23 : V :Vanadyum
24 : Cr :Krom
25 : Mn : Mangan
26 : Fe : Demir
27 : Co : Kobalt
28 : Ni : Nikel
29 : Cu : Bakır
30 : Zn : Çinko
31 : Ga : Galyum
32 : Ge : Germanyum
33 : As : Arsenik
34 : Se : Selenyum
35 : Br : Brom
36 : Kr : Kripton
37 : Rb : Rubidyum
38 : Sr : Stronsiyum
39 : Y : İtriyum
40 : Zr : Zirkonyum
41 : Nb : Niobyum
42 : Mo : Molibden
43 : Tc : Teknesyum
44 : Ru : Rutenyum
45 : Rh : Rodyum
46 : Pd : Paladyum
47 : Ag : Gümüş
48 : Cd : Kadmiyum
49 : In : İndiyum
50 : Sn : Kalay
51 : Sb : Antimon
52 : Te : Tellür
53 : I : İyot
54 : Xe : Ksenon
55 : Cs : Sezyum
56 : Ba : Baryum
57 : La : Lantan
58 : Ce : Seryum
59 : Pr : Praseodim
60 : Nd : Neodimyum
61 : Pm : Prometyum
62 : Sm : Samaryum
63 : Eu : Evropiyum
64 : Gd : Gadolinyum
65 : Tb : Terbiyum
66 : Dy : Disprozyum
67 : Ho : Holmiyum
68 : Er : Erbiyum
69 : Tm : Tulyum
70 : Yb : İterbiyum
71 : Lu : Lutetyum
72 : Hf : Hafniyum
73 : Ta : Tantal
74 : W : Volfram
75 : Re : Renyum
76 : Os : Osmiyum
77 : Ir : İridyum
78 : Pt : Platin
79 : Au : Altın
80 : Hg : Cıva
81 : Tl : Talyum
82 : Pb : Kurşun
83 : Bi : Bizmut
84 : Po : Polonyum
85 : At : Astatin
86 : Rn : Radon
87 : Fr : Fransiyum
88 : Ra : Radyum
89 : Ac : Aktinyum
90 : Th : Toryum
91 : Pa : Protaktinyum
92 : U : Uranyum
93 : Np : Neptünyum
94 : Pu : Plütonyum
95 : Am : Amerikyum
96 : Cm : Küriyum
97 : Bk : Berkelyum
98 : Cf : Kaliforniyum
99 : Es : Aynştaynyum
100 : Fm : Fermiyum
101 : Md : Mendelevyum
102 : No : Nobelyum
103 : Lr : Lavrensiyum
104 : Rf : Rutherfordiyum
105 : Db : Dubniyum
106 : Sg : Seaborgiyum
107 : Bh : Bohriyum
108 : Hs : Hassiyum
109 : Mt : Meitneriyum
110 : Ds : Darmstadtiyum
111 : Uuu : Ununnilyum
112 : Uub : Ununbiyum
113 : Uut : Ununtriyum
114 : Uuq : Ununkuadyum
115 : Uup : Ununpentiyum
116 : Uuh : Ununheksiyum
117 : Uus : Ununseptiyum
118 : Uuo : Ununoktiyum
119 : Uue : Ununenniyum
120 : Ubn : Unbiniliyum
(119 ve 120 atom numaralı elementler genişletilmiş periyodik tabloda yer almaktadır.)
Bu elementlerin 118 tanesi periyodik tabloda bulunuyor. Elementlerin isimleri en sağda, ortada sembolleri ve en solda ise atom numaraları yazmaktadır.
İLK 20 ELEMENT HANGİSİ?
- 1 : H : Hidrojen
- 2 : He : Helyum
- 3 : Li : Lityum
- 4 : Be : Berilyum
- 5 : B : Bor
- 6 : C : Karbon
- 7 : N : Azot
- 8 : O : Oksijen
- 9 : F : Flor
- 10 : Ne : Neon
- 11 : Na : Sodyum
- 12 : Mg : Magnezyum
- 13 : Al : Alüminyum
- 14 : Si : Silisyum
- 15 : P : Fosfor
- 16 : S : Kükürt
- 17 : Cl : Klor
- 18 : Ar : Argon
- 19 : K : Potasyum
- 20 : Ca : Kalsiyum
PERİYODİK TABLO NEDİR?
Periyodik tablo, kimyasal elementlerin sınıflandırılması için geliştirilmiş tablodur. Dilimizde periyodik tablo, periyodik cetvel, periyodik çizelge, elementler tablosu gibi birçok şekilde isimlendirilmiştir. Bu tablo bilinen bütün elementlerin artan atom numaralarına (buna proton sayısı da denir) göre bir sıralanışıdır. Periyodik cetvelden önce de bu yönde çalışmalar yapılmış olmakla birlikte, mucidi genelde Rus kimyager Dmitri Mendeleyev kabul edilir. 1869'da Mendeleyev atomları artan atom ağırlığına göre sıraladığında belli özelliklerin tekrarlandığını fark etti. Özellikleri tekrarlanan elementleri alt alta yerleştirdi ve buna periyot adını verdi.
Periyodik cetvelin görüntüsüne aşağıdan bakabilirsiniz:
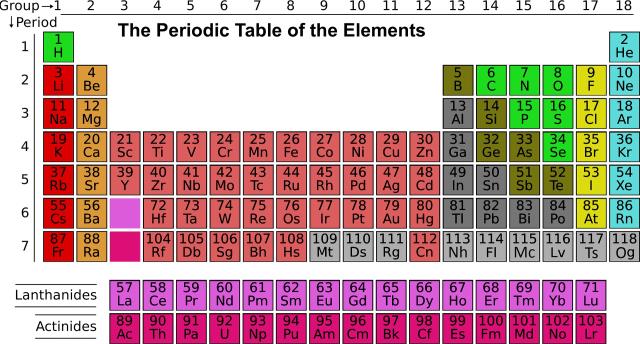
PERİYODİK TABLODA KAÇ ELEMENT VARDIR?
Normal periyodik tabloda 118 element bulunur. Genişletilmiş periyodik tabloda ise bazı kaynaklara göre 120 bazılarına göre ise 121 element bulunmaktadır. Tüm elementlerin isimlerini ve sembollerini yukarıda paylaşmıştık.
GENİŞLETİLMİŞ PERİYODİK TABLO NEDİR?
Periyodik tablonun 7. periyodun ilerisine genişletilmesi, atom numarası 118'den büyük olan kimyasal elementlerin periyodik tabloya kaydedilebilmesini sağlar. Bu tablo 8'inci ve (sonuç olarak) 9'uncu periyotları kapsar. Böyle bir tablo 1969'da Glenn T. Seaborg tarafından önerilmiştir. Standart periyodik tablonun, keşfedilmemiş elementleri kapsamak için ortaya konmuş bir uzantısıdır. Yeni periyotlar tam olarak 7. periyodun "kopyaları" değil, içinde bir de g-orbitali ile eklenen 18 elementi kapsayan bir de "g-bloğuna" sahiptirler. Bu kısımdaki yeni elementlerin hiçbiri henüz sentezlenmemiş ya da doğada keşfedilmemiştir. (Nisan 2008'de Element122'in doğada var olduğu söylenmiş fakat genel olarak hatalı bulunmuştur.) İlk g-bloğu elementinin atom numarası büyük ihtimalle 121 ve sistematik ismi unbiyunyumdur. Bu bölgedeki elementler büyük ihtimalle radyoaktif açıdan çok dengesizdir.
PERİYODİK TABLODA KAÇ GRUP VAR? A VE B GRUBU ELEMENTLER
Periyodik tabloda dikey sütunlara grup denir. Aynı grupta olan elementlerin kimyasal özellikleri benzerdir. Aşağı doğru dikeyce indikçe özellik yoğunlaşır ve belirginleşir. Bir A grubuna ait elementin son katmanında kaç elektron varsa grup sıralaması da odur. Örneğin, berilyum (Be) atomunun son katmanında 2 elektron vardır ve bu atom 2A grubunun elementi olur.
Bir gruptaki elementlerde yukarıdan aşağıya doğru inildiğinde Atom yarıçapı artar, iyonlaşma enerjisi ve elektronegatiflik ise azalır.
Periyodik tabloda 8 tane A 8 tane de B grubu vardır. A grubu elementlerine baş grup elementleri de denir. Bazı grupların özel adları şöyledir.
- 1A grubu Alkali metal'ler denir. Hidrojen hariç hepsi metaldir.
- 2A grubu Toprak alkali metalleri denir. Hepsi metaldir.
- 3A grubu Toprak metalleri (ya da Bor grubu) olarak adlandırılır.
- 4A Karbon grubu olarak adlandırılır.
- 5A Azot grubu (ya da nitrojen grubu) olarak adlandırılır.
- 6A Oksijen (ya da Kalkojen) grubu olarak adlandırılır.
- 7A grubu Halojenler olarak adlandırılır.
- 8A grubu Soygazlar bu grupta yer alır.
B grubu elementlerinin tamamı metaldir. B grubu elementlerine geçiş metalleri de denir. B grubunun 2 ilginç özelliği vardır. 2A grubu ile 3A grubu arasında yer alır.
1B den başlamaz. 3B ile başlar. (2A dan sonra geldiğinden) 2B ile biter.... (2B den sonra 3A gelir).
8B grubu yan yana 3 lü element gruplarından oluşur. 8B grubunda dikey benzerlikler yatay benzerliklerden daha önemlidir.
PERİYODİK TABLO GRUP NUMARALANDIRMA
Grupları numaralandırmanın üç yolu vardır. İlk kullanım Hindu-Arap Rakamları'nı kullanmak, diğer iki yöntem ise Roma rakamları'dır.
Avrupa ve Amerika'da kullanılan sisteme göre periyodik tablo grupları:
- 1. Grup (IA,IA): alkali metaller, hidrojen ya da lityum ailesi
- 2. Grup (IIA,IIA): alkali yer metalleri ya da berilyum ailesi
- 3. Grup (IIIA,IIIB): skandiyum ailesi
- 4. Grup (IVA,IVB): titanyum ailesi
- 5. Grup (VA,VB): vanadyum ailesi
- 6. Grup (VIA,VIB): krom ailesi
- 7. Grup (VIIA,VIIB): manganez ailesi
- 8. Grup (VIII): demir ailesi
- 9. Grup (VIII): kobalt ailesi
- 10. Grup (VIII): nikel ailesi
- 11. Grup (IB,IB): copper ailesi
- 12. Grup (IIB,IIB): çinko ailesi
- 13. Grup (IIIB,IIIA): bor ailesi
- 14. Grup (IVB,IVA): karbon ailesi
- 15. Grup (VB,VA): pentels ya da azot ailesi
- 16.Grup (VIB,VIA): kalkojen ya da oksijen ailesi
- 17. Grup (VIIB,VIIA): halojen ya da flor ailesi
- 18. Grup (Grup 0): soygaz ya da helyum ailesi

ELEMENTLERİN ÖZELLİKLERİ NELERDİR?
Elementlerin birçok özellikleri vardır. En önemli özellikleri aşağıdaki gibidir:
- Elementler tek tür atomdan oluşur. Mesela oksijen, karbon, demir gibi.
- Sembollerle gösterilir. Mesela Karbon (C) ve Oksijen (O) gibi.
- Günümüzde 118 elementin varlığı bilinmektedir. Fakat bazı kaynaklara göre toplamda 120 element bulunmaktadır. Bu elementlerden 92 tanesi doğal ve diğerleri ise yapaydır. Yani yapay olanlar laboratuvarda üretilmişlerdir.
- Doğada bulunan elementlerin çok az bir miktarı He ve Ar gibi atomik halde bulunur. Bazıları N2, O2, Cl2 gibi 2 atomlu (yani diatomik) halde bulunurken bazıları ise O3 ve S8 gibi çok atomlu (yani bir diğer adıyla poliatomik) yapıda bulunmaktadır. Birçok element ise NaCl, CaCO3 ve NO2 gibi bileşikli halde bulunmaktadır.
- Elementlerin tümü saf maddelerdir.
- Homojendirler.
- Belirli ayırt edici özellikleri mevcuttur. Örneğin erime noktası, kaynama noktası ve yoğunluk gibi.
- Kimyasal ve fiziksel yöntemlerle ayrıştırılamaz. Bileşikler ayrışabilir ama elementler saf madde oldukları için ayrıştırılamazlar.
- Genel olarak birçok element, bileşiklerinin kimyasal yöntemlerle ayrıştırılması sonucunda elde edilmektedir.
KİMYADAKİ EN ÖNEMLİ ELEMENT HANGİSİ?
Kimyada elbette birçok önemli element var. Fakat en önemli elementlerden birisi C Karbon'dur. Karbon elementi hemen hemen tüm maddelerde yer almaktadır. Doğada her yerde bulunur diyebiliriz. Dikkat ettiyseniz kimyasal çoğu bileşikte C (Karbon) yer almaktadır. Karbon çoğu element ile bileşiğe girebilmektedir. Karbonsuz yaşam düşünülemez...














